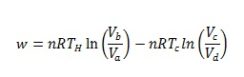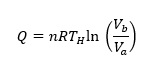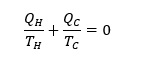Le Cycle De Carnot
LE CYCLE DE CARNOT, PROPOSÉ PAR L’INGÉNIEUR FRANÇAIS N. L. SADI CARNOT EN 1824, SE COMPOSE D’UNE SÉRIE DE QUATRE PROCÉDÉS RÉVERSIBLES. PARCE QUE LE CYCLE EST ENTIÈREMENT RÉVERSIBLE, IL EST LE MOYEN LE PLUS EFFICACE DE CONVERTIR LA CHALEUR FOURNIE AU SYSTÈME EN TRAVAIL UTILE.
D’autres exemples de cycles thermodynamiques sont le cycle de Brayton, le cycle d’Otto, le cycle de Diesel, le cycle de Rankine ou le cycle de Stirling, etc. Tous les cycles thermodynamiques sont les versions idéalisées des processus réels et sont étudiés pour comprendre les conceptions des systèmes les plus efficaces.
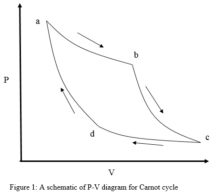
Pour le cycle de Carnot, les quatre états thermodynamiques du graphique pression-volume sont représentés par a, b, c et d(Figure 1). Le volume V est tracé sur l’axe des abscisses (X) tandis que la pression P est représentée sur l’axe des ordonnées (Y). Le cycle se compose de quatre étapes réversibles, à savoir
- a) Expansion isothermique – Avec l’ajout de chaleur, QH, le système se dilate et passe de l’état aà bà une température constante, TH. Puisque le processus est isothermique, le changement dans l’énergie interne, ΔU est zéro.
b) Expansion adiabatique – Le système passe de l’état b à c sans échange de chaleur avec l’environnement pendant que la température du système change à TC, où TC<TH. Comme le système est adiabatique de manière réversible, variation d’entropie, ΔS est égal à zéro.
c) Compression isothermique – Avec l’évacuation de la chaleur, QC, à une température constante TC, le système se comprime de l’état c à d. À nouveau, puisque le processus est isothermique, le changement dans l’énergie interne, ΔU est zéro.
b) Compression adiabatique – Le système comprime de d à a sans échange de chaleur avec l’environnement pendant que la température du système augmente de TC, à TH. Là encore, ΔS est égal à zéro car il s’agit d’un processus adiabatique réversible.
En utilisant les lois du gaz idéal, le travail total effectué par le système, w est donné par
où n et R sont le nombre de moles de gaz et la constante des gaz, respectivement. La chaleur fournie au système, QH est donnée par
(3) L’efficacité du cycle de Carnot, η est donnée par

En utilisant (1) – (3) et les expressions de gaz idéal pour les systèmes adiabatiques, on pourrait déduire que l’efficacité d’un système, η est donnée par (J.M. Smith, 2005)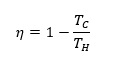 (4)
(4)
Par conséquent, plus la différence entre les réservoirs chaud et froid est grande, plus l’efficacité du cycle de Carnot est grande. Selon la deuxième loi de la thermodynamique, étant donné que toute la chaleur ajoutée au système ne peut pas être convertie en travail, l’efficacité de tout cycle thermodynamique ne peut jamais être de 100%. De plus, via (1) et (3), on peut en déduire que
où QC est négatif puisqu’il s’agit de la quantité de chaleur libérée.
Outre les hypothèses de la loi des gaz parfaits, le cycle de Carnot décrit ci-dessus repose sur d’autres hypothèses telles que l’absence de friction, de perte de chaleur, la réversibilité de chaque processus, le réservoir de chaleur infini, etc. Les processus réels utilisés dans les industries ont une efficacité bien moindre en raison des pertes d’énergie inhérentes au système. Par conséquent, le cycle de Carnot idéal a des applications pratiques limitées, sauf pour fournir le rendement théorique maximal atteint par un système. Néanmoins, il est important d’étudier le cycle car il constitue la base d’autres cycles thermodynamiques qui ont de nombreuses applications dans les industries. Deux des applications du cycle sont abordées ici, à savoir le moteur thermique à cycle de Carnot et la réfrigération.
Moteur thermique à cycle de Carnot
Le moteur thermique à cycle de Carnot est un moteur thermique hypothétique conçu sur la base du cycle Carnot dans lequel la chaleur transmise à un système est utilisée pour obtenir un travail mécanique utile. Sur la base du cycle de Carnot décrit ci-dessus, la chaleur produite est utilisée pour déplacer mécaniquement un piston qui est, à son tour, relié à une manivelle pour produire le mouvement/déplacement.
Réfrigération
La réfrigération est une méthode permettant d’évacuer la chaleur d’un environnement à basse température et de la dissiper dans un autre environnement à une température plus élevée. Comme discuté ci-dessus, elle implique quatre processus thermodynamiques qui constituent un cycle. Étant donné que ces processus sont réversibles, il est possible de faire le tour du cycle en sens inverse. Il se compose de quatre unités principales, à savoir une vanne d’étranglement, un évaporateur, un compresseur et un condenseur. Un liquide à haute température et à haute pression passe à travers une vanne d’étranglement qui réduit sa pression et sa température. Le liquide froid passe dans l’environnement pour être réfrigéré, où il absorbe la chaleur de l’environnement et se transforme en vapeur. Dans ce processus, le fluide en circulation absorbe la chaleur latente de l’environnement pour se vaporiser. Après avoir produit l’effet de refroidissement souhaité, la vapeur passe à travers un compresseur où elle est comprimée en vapeur à haute pression et à haute température. La dernière étape consiste à reconvertir la vapeur en liquide, ce qui se fait à l’extérieur du réfrigérateur, où la chaleur est dissipée dans l’environnement (atmosphère) et où la vapeur se condense en liquide. La haute température utilisée pour calculer l’efficacité maximale de Carnot dans ce cycle de réfrigération simple sera la température atmosphérique. Dans ce processus, la chaleur latente de vaporisation est éliminée du fluide en circulation. Le cycle se termine une fois que ce liquide à haute pression est introduit dans la vanne d’étranglement. Le principe de réfrigération est utilisé dans les industries ou dans les maisons pour la construction de réfrigérateurs et de climatiseurs.
J.M. Smith, H. V. (2005). Introduction to Chemical Engineering Thermodynamics. New York: McGraw Hill.